Страница: предыдущая последующая
СПОСОБЫ ПРЕДСТАВЛЕНИЯ СОСТАВА ВОД
ИСПОЛЬЗОВАНИЕ МИЛЛИГРАММ - ЭКВИВАЛЕНТА.
С целью упростить анализы состава вод результаты измерений концентраций компонентов, первоначально установленных в мг/л, принято выражать в грамм-эквивалентах на литр. Сокращенно миллиграмм-эквивалент на литр записывается в виде мг-экв/л.
Миллиграмм-эквивалент – число мг. химического элемента или соединения, равное весу его химического эквивалента.
Эквивалент химический – весовое количество химического элемента, соединяющееся с 1, точнее с 1,008, весовой частью водорода (или, соответственно с 8 весовыми частями кислорода); или замещающее 1 весовую часть водорода в соединениях.
Например, если в пробе воды обнаружено 20 мг хлора на 1 л. , то концентрация хлора в мг-экв/л, с учетом того, что относительная атомная масса хлора равна 35,5 составит: 20:35,5 = 0,56 мг-экв/л.
Для многовалентных элементов единица концентрации 1 мг-экв/л равна частному от деления относительной молекулярной массы на валентность.
Например, если концентрация в мг/л аниона HCO 3 определена равной 146,4 мг/л. , а молярная масса равна 60, то концентрация его в мг-экв/л окажется равной 146,4 / 60 = 2,44 мг-экв/л.
Формат таблицы для хранения справочных данных,необходимых для анализа, а также размещения результатов анализа выбран следующим
Формат таблицы himich_svoistva
|
Имя поля |
Содержание поля |
Тип поля |
|
|
Справочные данные |
|
|
Id _vech |
код вещества |
numeric |
|
gruppa |
группа вещества |
character |
|
formula |
химическая формула |
general |
|
name |
наименование вещества |
character |
|
moljrn |
молярная масса |
numeric |
|
mg_ekv |
мг-экв/л |
numeric |
|
|
Экспериментальные данные |
|
|
mg_ekv_exp |
количество в мг-экв/л |
numeric |
|
mg_l_exp |
количество в мг/л |
numeric |
|
|
Расчетные данные |
|
|
mg_ekv_rach |
количество в мг-экв/л |
numeric |
|
mg_l_rach |
количество в мг/л |
numeric |
Таблиц содержит данные для решения следующих задач:
Таблица himij.dbf в BROWSE – окне представлена ниже

Основное достоинство миллиграмм- эквивалентных единиц то, что они являются международными.
ГРАФИЧЕСКОЕ ОТОБРАЖЕНИЕ ХИМИЧЕСКОГО СОСТАВА ПРИРОДНЫХ ВОД
Упрощенная диаграмма – прямоугольник – прямоугольник, горизонтальный или вертикальный делится пополам и в каждой из половинок отображается по три участка для анионов и катионов, которые наносятся в масштабе в мг-экв/л, где затем можно выделить характеристики жесткости, щелочности природной воды и решить ряд аналитических задач:
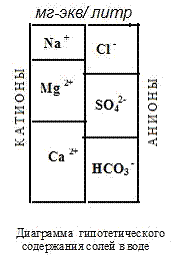
1. Определить общую и карбонатную жесткость воды:
· общую жесткость, как сумму концентраций ионов Ca 2+ и Mg 2+ ,
[ОЖ] = [Сa 2+] + [Mg 2+]
· карбонатную жесткость,
[КЖ] = [Ca 2+] + [Mg 2+] – [HCO 3-]
· общая и карбонатная жесткости равны, если катионы жесткости полностью компенсированы анионами HCO 3- ,
[ОЖ] = [КЖ], если [Ca 2+] + [Mg 2+] =< [HCO 3-]
Щелочность определяется концентрацией ионов HCO 3- (если других слабых кислот не обнаружено):
· щелочность и карбонатная жесткость равны, если:
[HCO 3-] =< [Ca 2+] + [Mg 2+]
Пользуясь диаграммой можно определить правильность выполнения химического анализа.
В базе BROWSE – окне анализа параметров, определяющих щелочность, имеет следующую структуру:
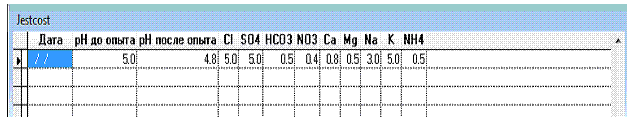
ФОРМИРОВАНИЕ УПРОЩЕННОЙ ЖИМИЧЕСКОЙ ФОРМУЛЫ
Простейшая химическая формула (БСЭ 35) – химическая формула, отражающая наиболее простой атомный состав данного вещества, в то время как истинная формула, содержит истинное число, из которых состоит молекула вещества.
Чтобы сформировать простейшую химическую формулу сложного химического индивида весовое процентное содержание каждого из элементов, входящего в его состав делят на атомный вес соответствующего элемента. Затем полученные частные от деления делят на наименьшее из них или на число кратное ему и округляют до целых чисел, выражающих простейший атомный состав сложного вещества.
Например, углеводород этилен состоит из 85,63 % углерода и 14,37 % водорода. Зная, что атомный вес С = 12,01 и H = 1,008, получаем частные от деления : 18,63 : 12,01 = 7,129 и 14,37 : 1,008 = 14,259. Далее, 7,29 : 14,259 = 1 : 2. Следовательно, этилен на 1 атом углерода содержит 2 атома водорода: пролстейшая формула его будет : CH 2 . Но плотность углерода по отношению к водороду равна 13,9, поэтому молекулярный вес этилена равен 13,9 : 2,016 = 28,2.
Определяющее влияние на свойства воды оказывают соединения угольной кислоты H2CO3 ( слабая двухосновная кислота). При растворении в воде углекислого газа (CO 2) происходит его частичное взаимодействие с водой, ведущее к образованию угольной кислоты (см. п. 2) , Равновесие этой реакции смещено влево, особенно при повышенной температуре. Прибавление щелочи смещает равновесие вправо.
Угольная кислота образует два ряда солей: средние углекислые (с анионом CO 3 2 -) – карбонаты и кислые углекислые (с анионом HCO 3 - ) – бикарбонаты.
В карбонатно – кальциевой системе присутствуют ионы водорода, поэтому на соотношение компонентов системы влияет величина pH.
Карбонатно – кальциевая система – неустойчивая система. В условиях ее равновесия определенной концентрации бикарбонатов (HCO 3 -) соответствует определенное количество свободной углекислоты , называемой равновесной. Вода при этом стабильна (не происходит ни выпадения карбонатов (CaCO 3), ни их дополнительного растворения).
Если количество растворенной углекислоты больше ее равновесной концентрации, равновесие реакции (7) сдвинется вправо,
что приведет к к растворению CaCO 3. Избыток CO 2 сверх равновесной концентрации называется агрессивной углекислотой. Контакт агрессивной воды с бетоном приводит к вымыванию из него карбоната кальция.
При недостатке CO
2 по сравнению с равновесной реакция (7) протекает справа налево, что
приводит к дополнительному и выпадению в осадок малорастворимого карбоната
кальция. ![]()
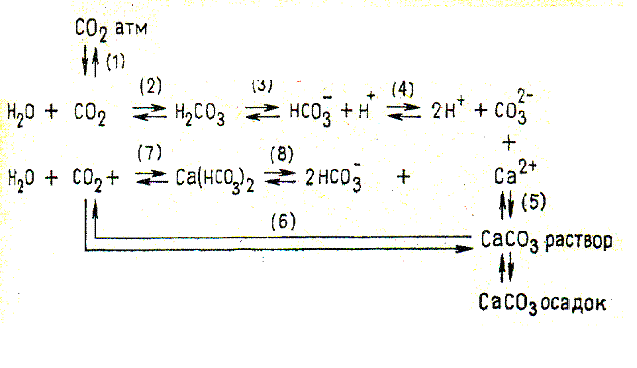
Рис 2.1.Карбонатно – кальциевая система в природных водах
Стабильность воды может быть оценена экспериментально или вычислением индекса насыщения воды карбонатом кальция по результатам определения температуры воды, общего солесодержания, концентрации ионов кальция и общей щелочности.
ТРЕБОВАНИЯ К ВОДАМ НЕЦЕНТРАЛИЗОВАННОГО ВОДОСНАБЖЕНИЯ
Требований, предъявляемых к воде хозяйственно – питьевого назначения немного: она должна быть безвредной в эпидемиологическом отношении, по химическому составу и иметь удовлетворительное качество по вкусу и цвету.
Главным в оценке качества волы нецентрализованного водоснабжения (из колодца, родника, скважины) являются свойства безопасности, которыми являются условие невыхода норм за установленные показатели.
Ниже приведены рекомендуемые отечественными нормативными документами требования к качеству питьевой воды, а также регламентами Всемирной организации здравоохранения (ВОЗ) и Европейским сообществом ЕС
|
Показатели качества |
Един. изм. |
ГОСТ 2874-82 |
СанПиН 2.1.4.559-96 |
ВОЗ |
ЕС |
|
Органолептические (не более) |
|
|
|
|
|
|
Запах при 20 0 С |
баллы |
2 |
2 |
- |
- |
|
Привкус при 20 0 С |
баллы |
2 |
2 |
- |
- |
|
Мутность |
мг/л |
1,5 |
1,5 |
2,8 |
2,3 |
|
Цветность |
град |
20 |
20 |
15 |
20 |
|
Обобщенные показатели |
|
|
|
|
|
|
Водородный показатель, pH |
относ. |
6,0-9.0 |
6,0-9,0 |
6,5-8,5 |
6,5-9,5 |
|
Общая жесткость |
мг-экв/л |
<=7 |
<=7 |
- |
<=50 |
|
Перманганантная окисляемость |
мгО/л |
<=5 |
<=5 |
- |
<=5 |
|
ХПК |
мгО/л |
- |
<=15 |
- |
- |
|
Сухой остаток |
мг/л |
<=1000 |
<=1000 |
- |
- |
|
Проводимость |
мкСим/см |
- |
- |
- |
<=2500 |
|
Щелочность общая |
мг-экв/л |
- |
<=7 |
- |
- |
|
Химические показатели, не более |
|
|
|
|
|
|
Алюминий |
мг/л |
0,5 |
0,5 |
- |
- |
|
Аммоний |
мг/л |
- |
0,5 |
- |
0,5 |
|
Железо Fe общ /Fe 2+ |
мг/л |
0,3 |
0,3 |
0,3 |
0,2 |
|
Марганец |
мг/л |
0,1 |
0,1 |
0,1-0,5 |
0,5 |
|
Натрий |
мг/л |
- |
200 |
- |
200 |
|
Кальций |
мг/л |
- |
30-140 |
- |
- |
|
Судьфаты /SO/ |
мг-экв/л |
500 |
500 |
250 |
250 |
|
Хлориды /Cl/ |
мг-экв/л |
350 |
350 |
250 |
250 |
|
Нитраты /по NO/ |
мг-экв/л |
45 |
45 |
50 |
50 |
|
Нитриты /ион/ |
мг-экв/л |
0,1 |
3,0 |
- |
0,5 |
|
Фосфаты /P)/ (полифосфаты) |
мг-экв/л |
|
|
|
|
|
Силикаты /активированные/ |
мгSi/л |
- |
10 |
- |
- |
|
Фториды /F/ |
мг/л |
- |
0,7-1,5 |
1,5 |
O,7-1,5 |
|
Бикарбонаты |
мг/л |
- |
400 |
- |
- |
|
Растворенный кислород |
мг/л,%нас |
- |
>50% |
- |
>50% |
|
Азот аммонийный |
мг/л |
- |
1,5 |
- |
- |
|
Кремний /Si/ |
мг/л |
- |
10 |
- |
- |
|
Медь /Cu/ |
мг/л |
1 |
1 |
- |
2 |
|
Свинец |
мг/л |
0,03 |
0,03 |
- |
0,01 |
|
Мышьяк /As/ |
мг/л |
- |
0,05 |
- |
- |
|
Молибден /Mo/ |
мг/л |
0,25 |
0,25 |
- |
- |
|
Кадмий |
мг/л |
- |
0,001 |
- |
0.005 |
|
Цинк /Zn/ |
мг/л |
5 |
5 |
- |
- |
|
Магний |
мг/л |
- |
20-50 |
- |
- |
|
Беррилий |
мг/л |
0,0002 |
- |
- |
|
|
Селен |
мг/л |
0,0001 |
- |
- |
0,0001 |
|
Стронций |
мг/л |
7 |
- |
- |
- |
|
Никель |
мг/л |
- |
0,1 |
- |
- |
|
Хром |
мг/л |
- |
0,5 |
- |
0,5 |
|
Полиакриламид остаточный |
мг/л |
2 |
- |
- |
- |
|
Свободная углекислота |
мг/л |
- |
80 |
- |
- |
|
Свободный хлор |
мг/л |
- |
0,3-0,5 |
- |
- |
|
Сероводород /HS/ |
мг/л |
- |
0,003 |
- |
- |
|
Биологические показатели |
|
|
|
|
|
|
Термотоперантные колиформные бактерии |
число в 100 мл |
- |
отсутствие |
отсутствие |
отсутствие |
|
Общие колиформные бактерии |
число в 100 мл |
- |
отсутствие |
отсутствие |
отсутствие |
|
Число бактерий группы кишечных палочек в 1 л воды /коли-индекс/ |
|
до 3 |
- |
- |
- |
|
Число микроорганизмов в 1 см 3 воды |
|
До 100 |
- |
- |
- |
|
Фенольный индекс |
мг/л |
- |
0,25 |
- |
- |
|
СПАВ |
мг/л |
- |
0,5 |
- |
- |
С целью обеспечения постоянства качества воды , безопасности водоснабжения населения нормативными документами предусмотрено систематическое обследование качества вод, которое должно соответствовать требованиям, представленным таблицей:
Требования к качеству вод нецентрализованного водоснабжения (СанПиН 2.1.4.1175 - 02)
|
Показатель |
Единица измерения |
Норматив |
|
|
Органические вещества |
|
||
|
Запах |
баллы |
<= 2 - 3 |
|
|
Привкус |
баллы |
<= 2 - 3 |
|
|
Цветность |
градусы |
<= 30 |
|
|
Мутность |
ЕМФ (ед мутности по формазину), или мг/л (по кофлину) |
2,6 – 3,5 <= 1,5 - 2 |
|
|
Химические вещества |
|
||
|
Водородный показатель |
Ед. pH |
6 - 9 |
|
|
Жесткость (общая) |
мг-экв/л |
7 - 10 |
|
|
Нитраты (N0 …) |
мг/л |
<= 45 |
|
|
Общая минерализация (сухой остаток) |
мг/л |
<= 1000 - 1500 |
|
|
Окисляемость (перманганатная) |
мг/л |
<= 5 - 7 |
|
|
Сульфаты (SO …) |
мг/л |
<= 500 |
|
|
Хлориды (Cl …) |
мг/л |
<= 350 |
|
|
Химические веществава органической и неорганической природы |
мг/л |
ПДК |
|
|
Микробиологические |
|
||
|
Общие колиформные бактерии |
число бактерий в 100 мл |
отсутствие |
|
|
Общее микробное число |
число образующих колоний в 1 мл |
100 |
|
|
Термотолерантные колиформные бактерии |
число бактерий в 100 мл |
отсутствие |
|
|
Колифаги |
Число бляшкообразующих единиц |
отсутствие |
|
Специализированными аналитическими лабораториями обычно предлагаются 3 вида анализа качества вод: анализ (9 – 11 показателей), стоимостью 1,5 – 2 тыс. рубл.; полный химический анализ (22 – 24 показателя), стоимостью 2 – 2,5 тыс. руб. ; определение отдельных показателей по желанию заказчика. Финансирование этой система предполагается из бюджетов местных муниципальных органов (таких сумм там пока не найдется, как правило), из бюджетов садоводств , где таких средств никогда не было, или частными владельцами, которые не убеждены, что это надо делать (традиционный “авось”). Подорвать незыблемость упомянутого “авось” можно, если вооружить местные системы управления экспресс – методами, позволяющими, пусть не выполнить качественный химический анализ в объеме двух – трех десятков показателей, для чего необходима хорошо оснащенная лаборатория, но своевременно, силами, например, уполномоченного ( может иметь соответствующую подготовку), убедиться что он крайне необходим. Решению этих проблем и посвящена данная работа.
В приложении “Управление качеством нецентрализованного водоснабжения” данные, касающиеся контроля качества вод, сформируем в виде четырех реляционных таблиц c аналогичными структурами, которые представим в BROWSE – формате.
1. Органолептические свойства (control_organolept.dbf):

2. Химические свойства (control_himij.dbf):

3. Обобщенные свойства (сщтекщд_щищисрутювиа):

4. Биологические свойства (control_bio):

Четыре базовых таблицы дополняются необходимым количеством представлений данных для анализов в необходимом ключе, что будет описано в разделе “Интерфейс приложения”.
Страница: предыдущая последующая